תוֹכֶן
במאמר זה: איזון משוואה בשיטת ניסוי וטעייה איזון משוואה בשיטה האלגברית סיכום המאמר הפניות
בכימיה, משוואה קובעת את מה שקרה במהלך תגובה כימית. משמאל למשוואה, אנו ממקמים את הריאגנטים ששימשו לניסוי ומימין, את המוצרים שהתקבלו במהלך הניסוי. על פי העיקרון של שימור המסה (לבואה) במהלך תגובה כימית, שום אטום לא נעלם, אף אחד לא נוצר, הם משתלבים בצורה שונה. לסיכום, עליך להיות בעל אותם מספר תאומים של כל אלמנט מימין לזה שמשמאל למשוואה. לכן תמיד חייבים להיות מאוזנים משוואת איזון.
בשלבים
שיטה 1 איזון משוואה בשיטת ניסוי וטעייה
-
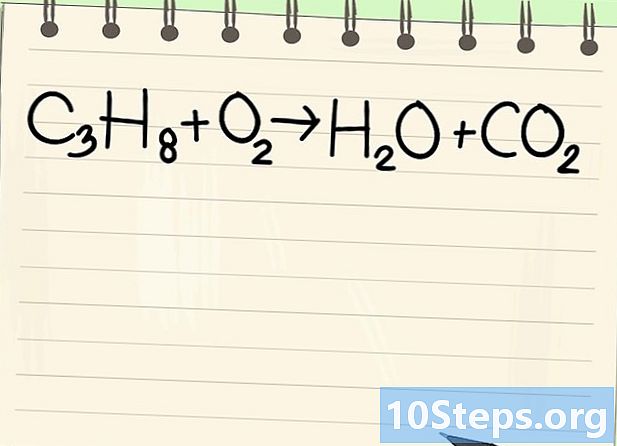
שימו לב למשוואת האיזון. נתייחס למשוואה הבאה:- ג3H8 + O2 -> ח2O + CO2
- זו המשוואה של בעירה פרופאן (C3H8) בחמצן: מתקבלים מים ופחמן דו חמצני.
-
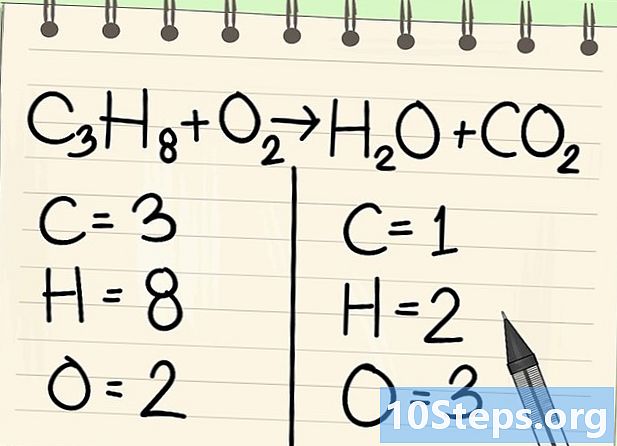
לספור את האטומים. הזן את מספר הדאטומים של כל אלמנט בצד אחד של המשוואה ואז את השני. לשם כך, קח בחשבון את המדדים, אם אין כאלה, המדד הוא 1.- בצד שמאל ישנם 3 אטומי פחמן, 8 מימן ו -2 חמצן.
- בצד ימין יש אטום אחד של פחמן, 2 של מימן ושלושה של חמצן.
-
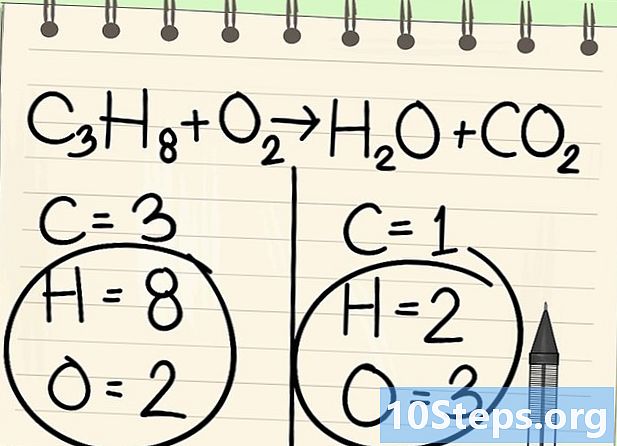
השאירו בצד לרגע את המימן והחמצן. -

התחל לאזן עם האלמנט הנכון. אנחנו תמיד מתחילים בזה שנמצא במולקולה לפני התגובה ואחריה. אם יש כמה, קח את זה שהוא חד-ערכי באחת המולקולות. כאן נתחיל באטומי הפחמן. -

איזון אטומי הפחמן. הוסף מימין מקדם למולקולת הפחמן הדו-חמצני (CO2) בו לוטום הפחמן נמצא לבדו. אנו שמים 3 כדי לקבל את 3 האטומים השמאלים.- ג3H8 + O2 -> ח2O + 3CO2
- לפיכך יש לנו 3 אטומי פחמן מימין בזכות המקדם (3CO2) ו -3 אטומי פחמן משמאל בזכות המדד (C3H8).
- במשוואה אתה יכול לשים את כל המקדמים שאתה רוצה, אבל אתה לא יכול לגעת ברמזים.
-
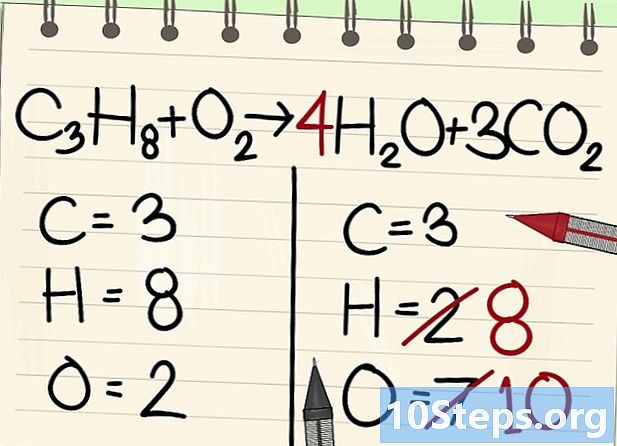
איזון אטומי המימן. כשיש לך 8 שמאל מהמשוואה, אתה זקוק לא פחות מימין.- ג3H8 + O2 --> 4H2O + 3CO2
- בצד ימין תציב מקדם 4, מכיוון שהמימן הוא דו-ערכי במולקולת המים: המדד 2 מציין ששני אטומי מימן קשורים.
- כדי להשיג את מספר אטומי המימן מימין, מכפילים את המקדם 4 במדד 2, או 8 אטומים.
- באשר לאטומי החמצן, בצד ימין, ישנם כעת 6 בצד אחד, המגיעים משלוש המולקולות של 3CO2 (3 x 2 = 6 אטומים) ו -4 מתוך 4 המולקולות של 4 H2O (4 x 1 = 4 אטומים), כלומר בסך הכל 10 אטומי חמצן.
-
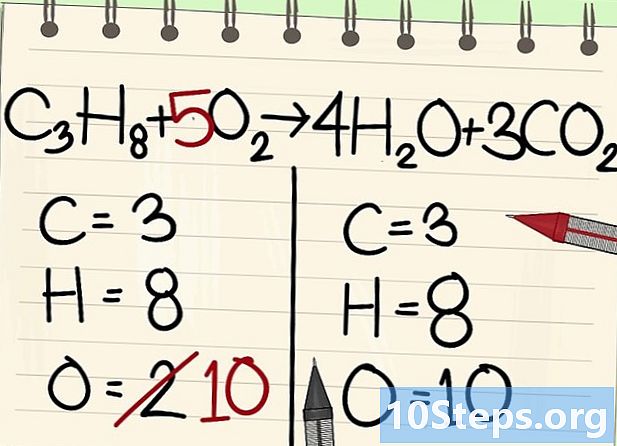
איזון אטומי החמצן.- בגלל איזון הפחמן והמימן, מספר אטומי החמצן אינו זהה משני צידי המשוואה. ראינו בעבר שיש מימין 10 אטומי חמצן (4 ממולקולות מים, ו -6 ממולקולות פחמן דו חמצני). בצד שמאל, יש רק 2 (מ- O2).
- כדי לאזן את החמצן, הוסף מקדם של 5 למולקולת החמצן השמאלית: יש לך 10 אטומי חמצן בצד שמאל והשני בצד ימין.
- ג3H8 + 5O2 -> 4 ח2O + 3CO2
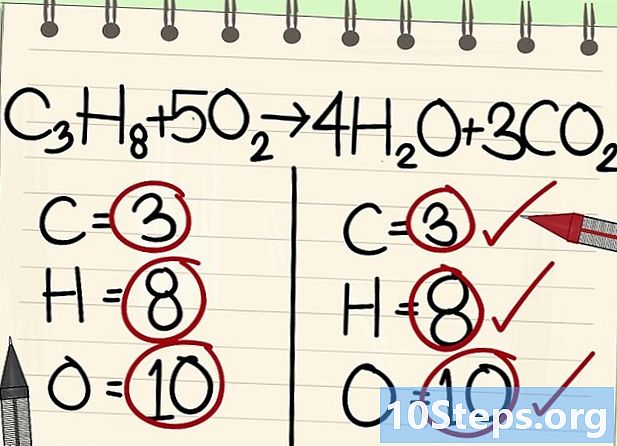
- כל האטומים (פחמן, מימן וחמצן) מאוזנים: המשוואה שלך מאוזנת.
שיטה 2 לאזן משוואה בשיטה האלגברית
-

כתוב את המשוואה לאיזון. הקצה לכל מולקולה מקדם מילולי. נתקשר אליהם יש, ב, ג ו ד. -
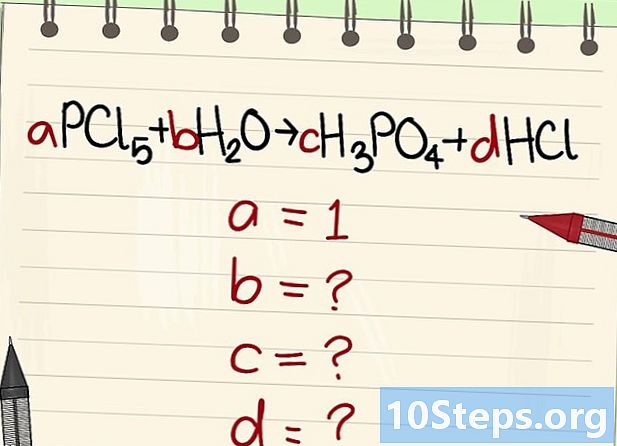
מצא את הערך של המקדמים המילוליים האחרים. נשאל זאת יש = 1. -

מצא את מערכות היחסים בין מקדמים אלה. במבט שמאלה (ריאגנטים) וימין (מוצרים), ביססו את הקשר בין מקדמים שונים אלה.- קחו את המשוואה הבאה: aPCl5 + bH2O = cH3PO4 + dHCl. נאמר כי a = 1, כלומר c = a, d = 5a ו- 2b = 3c + d. חישובים שנעשו, c = 1, d = 5 ו- b = 4.

- קחו את המשוואה הבאה: aPCl5 + bH2O = cH3PO4 + dHCl. נאמר כי a = 1, כלומר c = a, d = 5a ו- 2b = 3c + d. חישובים שנעשו, c = 1, d = 5 ו- b = 4.